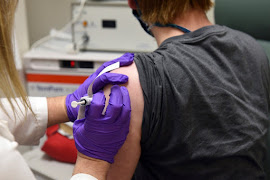
Al aumentar los casos de coronavirus en EE.UU y en otros lugares y con poco alivio a la vista, el mundo recibió buenas noticias el lunes. Pfizer y su socia, la compañía alemana BioNTech, anunciaron resultados preliminares que sugieren que su vacuna tiene una eficacia superior al 90 por ciento.
La noticia —los primeros resultados de cualquier ensayo de vacuna en la última etapa— animaron a los mercados de valores y a los espíritus al percibirse un rayo de esperanza. Pero vale la pena señalar que las noticias son aún preliminares, y hay mucho que todavía no se sabe sobre el funcionamiento de la vacuna.
Y una cosa quedó clara: la vacuna no llegará a tiempo para rescatar al mundo en los próximos meses, cuando el virus se llevará muchas más vidas a menos que el público tome medidas de salud pública más estrictas.
A continuación, lo que sabemos, y lo que no sabemos, sobre la vacuna.
Que descubrieron estos cientificos
Pfizer y BioNTech iniciaron un ensayo clínico en la última etapa de una vacuna contra el coronavirus. La mitad de las personas recibieron la vacuna, mientras que la otra mitad recibió un placebo de agua salada. Las compañías esperaron a que la gente se enfermara para determinar si la vacuna ofrecía alguna protección.
Hasta ahora, 94 participantes de casi 44.000 se han enfermado de COVID-19. Una junta independiente de expertos analizó cuántas de esas personas recibieron la vacuna y cuántas el placebo. Ese análisis temprano sugiere que la vacuna tiene una eficacia superior al 90 por ciento.
Como es habitual en los ensayos clínicos, los datos fueron “cegados”, lo que significa que nadie, excepto la junta independiente —ni los voluntarios, ni los médicos, ni los altos ejecutivos de la compañía— sabe cuántas de las 94 personas enfermas por el virus recibieron la vacuna o el placebo. Sin embargo, dado que se estima que la vacuna tiene una efectividad superior al 90 por ciento, podemos asumir con seguridad que muy pocas personas que fueron vacunadas se enfermaron de COVID-19.
Es ese un buen resultado?
Así es. La Administración de Alimentos y Medicamentos (FDA por su sigla en inglés) había establecido un límite de eficacia del 50 por ciento para los fabricantes de vacunas que quisieran presentar sus candidatas para una autorización de emergencia. Si los resultados preliminares de Pfizer y BioNTech se confirman —y reflejan con precisión cómo funcionará la vacuna en el mundo real— entonces es mucho más protectora que eso.
Para tener una idea de lo buenos que son estos resultados, vale la pena considerar las vacunas autorizadas que la gente recibe regularmente. En el extremo inferior, las vacunas contra la gripe tienen una eficacia de entre el 40 y el 60 por ciento como mucho, porque el virus de la gripe evoluciona en nuevas formas año tras año. Por el contrario, dos dosis de la vacuna contra el sarampión tienen una eficacia del 97 por ciento.
Si la vacuna recibe una autorización de emergencia de la FDA y se distribuye a millones de personas, los Centros para el Control y la Prevención de Enfermedades de Estados Unidos y la FDA la monitorearán para asegurarse de que no haya evidencia de problemas de seguridad aún más raros.
Los participantes en el ensayo también serán monitoreados durante dos años.
Quien recibirá primero la nueva vacuna?
El director general de Pfizer ha dicho que podría tener de 30 a 40 millones de dosis de la vacuna antes de fin de año, suficiente para que entre 15 y 20 millones de personas reciban una primera inyección y un refuerzo tres semanas después.
Aún no se ha decidido exactamente quiénes tendrán derecho a las dosis iniciales, pero es probable que reciban prioridad los grupos que corren un mayor riesgo de infección o que son más vulnerables al virus. Eso podría incluir a los trabajadores de la salud, así como a los adultos mayores y a los que tienen factores de riesgo como obesidad o diabetes.
Pfizer y BioNTech dicen que podrían aumentar su capacidad hasta alcanzar 1.300 millones de dosis al año. Eso está lejos de ser suficiente para satisfacer la necesidad mundial de vacunas. Si otras vacunas también resultan efectivas, las compañías podrán fabricarlas también y ayudar a satisfacer la demanda.
Cuando estará disponible para el publico en general?
Pfizer ha dicho que probablemente solicitará una autorización de emergencia en la tercera semana de noviembre, después de que reúna los dos meses de datos de seguridad que la FDA ha pedido a los fabricantes. Luego, la agencia consultará con un comité asesor externo de expertos. Puede tomar semanas analizar los datos detallados sobre la seguridad y la eficacia de la vacuna así como aumentar la capacidad de las compañías para fabricar millones de dosis de manera segura.
La vacuna podría autorizarse para ciertas poblaciones de alto riesgo antes de fin de año, pero eso solo sucedería si todo va como se ha planeado y no hay retrasos imprevistos.
Aunque los resultados preliminares ofrecen algunas pruebas convincentes de que la eficacia de la vacuna, no nos dicen con certeza cuán eficaz es. Los ensayos clínicos simplemente no están preparados para hacer eso. Solo pueden permitir a los científicos hacer una estimación basada en estadísticas, una estimación conocida como eficacia. La eficacia de una vacuna solo puede determinarse firmemente una vez que millones de personas la reciben. Pero los expertos dicen que los datos preliminares indican que la eficacia debería ser muy alta.
Funcionara en las personas mayores?
Los nuevos resultados tampoco nos dicen si las personas mayores obtendrán una fuerte protección de la vacuna. El ensayo clínico de Pfizer y BioNTech incluye a personas de más de 65 años, así que tarde o temprano proporcionará esta información crucial. Los primeros estudios clínicos han sugerido que las personas mayores producen una respuesta inmunológica más débil a las vacunas contra el coronavirus. Pero, al contar con una evidencia preliminar tan robusta, es posible que aún obtengan una fuerte protección de la vacuna.
Y los niños?
Otra pregunta que está en el aire es si los niños obtendrán protección de la vacuna. El ensayo llevado a cabo por Pfizer y BioNTech inicialmente estaba abierto a personas de 18 años o más, pero en septiembre comenzaron a incluir a adolescentes desde los 16 años. El mes pasado lanzaron un nuevo ensayo con niños de tan solo 12 años y planean llegar a edades más tempranas.
La vacuna de Pfizer fue parte de la OperacionVelocidad Maxima del gobierno
El lunes, el vicepresidente Mike Pence dijo en Twiter que la noticia llego “gracias a la asociación público-privada forjada” por Trump.
En julio, Pfizer consiguió un acuerdo de 1950 millones de dólares con la Operación Máxima Velocidad del gobierno, el esfuerzo de varias agencias para llevar de forma rápida una vacuna al mercado y entregar 100 millones de dosis de la vacuna. Es un acuerdo de compra por adelantado, lo que significa que la compañía no recibirá el pago hasta que entreguen las vacunas. Pfizer no aceptó fondos federales para ayudar a desarrollar o fabricar la vacuna, a diferencia de los líderes Moderna y AstraZeneca.
Pfizer se ha distanciado de Trump y de la Operación Máxima Velocidad. En una entrevista realizada el domingo, Kathrin Jansen, vicepresidenta principal y jefa de investigación y desarrollo de vacunas de Pfizer, dijo: “Nunca fuimos parte de Máxima Velocidad”, y añadió: “nunca hemos aceptado dinero del gobierno de Estados Unidos, ni de nadie”.
El lunes, una portavoz de Pfizer aclaró que la compañía es parte de la Operación Máxima Velocidad como proveedora de una potencial vacuna contra el coronavirus.
Aunque es cierto que Pfizer y BioNTech habían trabajado en una vacuna todo el año antes de que las compañías llegaran a un acuerdo con el gobierno de EE.UU. en julio, un acuerdo de 1950 millones de dólares es, sin embargo, un incentivo importante para seguir adelante. De hecho, las organizaciones internacionales de la salud han utilizado durante mucho tiempo estas garantías de mercado para alentar a los fabricantes con fines de lucro a suministrar vacunas a los paises en desarollo.
Que significa esta noticia para las otras vacunas en competencia?
Hay otras 10 vacunas en todo el mundo que están en la última fase de prueba. Que Pfizer y BioNTech hayan obtenido resultados alentadores hace que los expertos se sientan optimistas sobre el panorama.
“Nos da más esperanza de que otras vacunas también serán efectivas”, dijo Akiko Iwasaki de la Universidad de Yale.
Pfizer y BioNTech están probando una vacuna que utiliza una molécula genética llamada ARN para hacer que nuestras propias células produzcan una proteína viral. Nuestro sistema inmunológico se encuentra con la proteína y produce anticuerpos y células inmunológicas que pueden reconocer la proteína rápidamente y realizar un ataque rápido. Moderna se encuentra en la última etapa de las pruebas con una vacuna de ARN propia, y las primeras pruebas clínicas con otras vacunas de ARN están en marcha en China, Inglaterra, India, Singapur, Corea del Sur y Tailandia.
Pero las noticias de Pfizer y BioNTech también podrían ser alentadoras para otros desarrolladores de vacunas. La vacuna de Pfizer y BioNTech hace que nuestros cuerpos produzcan una proteína viral llamada espiga. Un número de otras vacunas llevan la proteína de espiga al cuerpo, o solo un fragmento de ella, para que el sistema inmunológico la reconozca. Otras vacunas se basan en otros virus, que introducen inofensivamente en las células un gen para la proteína de espiga. Si la proteína de espiga provoca una fuerte protección al coronavirus, entonces todas estas vacunas podrían también dar resultados alentadores en los próximos meses.
El éxito generalizado de las vacunas contra el coronavirus sería una gran ayuda para la salud mundial, porque Pfizer y BioNTech por sí solas no pueden satisfacer toda la demanda.
Ya podemos dejar de usar mascarillas?
Por favor, no lo hagas. El coronavirus está causando estragos en todo Estados Unidos y los expertos en salud pública han dicho que los estadounidenses deben estar preparados para un invierno muy duro.
Aunque se autorice una vacuna dentro de unos meses, inicialmente solo estará disponible para una pequeña parte del público estadounidense. La mayoría de los funcionarios de salud piensan que no habrá una vacuna efectiva disponible para cualquiera que así lo desee hasta bien entrado el año próximo. Incluso entonces, todavía no hay datos sobre si una vacuna detendrá la propagación asintomática del virus, o la medida en que evitará que las personas desarrollen COVID-19 grave.
La mayoría de los expertos dicen que incluso cuando una vacuna esté ampliamente disponible, las medidas adicionales como las mascarillas seguirán siendo necesarias hasta que la amenaza a la salud pública haya disminuido.
“Esto no reemplazará las medidas higiénicas, será un complemento de las medidas higiénicas”, dijo Paul Offit, profesor de la Universidad de Pensilvania y miembro del panel asesor de vacunas de la FDA. “Le debes a los demás el asegurarte de usar una mascarilla”.
New York Times